Tal como el "metro" es una unidad de medida de la longitud, y un "litro" es una unidad de medida de volumen de un líquido, el pH es una medida de la acidez o de la alcalinidad de una sustancia.
Los productos químicos que utilizamos a diario tienen un grado de acidez que podría ser peligroso. La única manera de probarlo sería midiendo el nivel del pH.
Hace mucho tiempo, los científicos querían medir el grado de acidez de una sustancia, entonces desarrollaron el concepto del pH. El pH (con la “p” en minúsculas) es una escala que nos sirve para medir si una sustancia es más ácida que otra y viceversa.
Robert Boyle, un químico aficionado irlandés del siglo 17, fue el primer científico en categorizar las soluciones como ácidas o alcalinas. Aunque varios científicos pulieron las definiciones de Boyle, la escala de pH no fue inventada hasta 1909 cuando el bioquímico danés Sören Sörensen creo una formula para medir la acidez.
Se ha
determinado que el pH de la piel húmeda ronda en un 5.5 por lo que si
nos aplicamos alguna crema o jabón con un pH menor o mayor podría
causarnos irritación o quemadura.
Si se tratara de un pH mayor a 10 o menor a 3, la piel pudiera disolverse causándonos un gran daño. Saber cuál es el pH de las sustancias es muy importante para nuestra seguridad ante cualquier producto químico.
Si se tratara de un pH mayor a 10 o menor a 3, la piel pudiera disolverse causándonos un gran daño. Saber cuál es el pH de las sustancias es muy importante para nuestra seguridad ante cualquier producto químico.
El pH es una medida utilizada por la química para evaluar la acidez o
alcalinidad de una sustancia por lo general en su estado líquido (también se
puede utilizar para gases). Se entiende por acidez la capacidad de una sustancia
para aportar a una disolución acuosa iones de hidrógeno, hidrogeniones (H*) al medio. La alcalinidad o base aporta hidroxilo OH-
al medio. Por lo tanto, el pH mide la concentración de iones de hidrógeno de una
sustancia, a pesar de que hay muchas definiciones al respecto.
La medición de la acidez y la alcalinidad es importante, pero ¿cómo está relacionado el pH con estas medidas?
Escala de pH
Los ácidos y las bases
tienen una característica que permite medirlos: es la concentración
de los iones de hidrógeno (H+). Los ácidos fuertes tienen altas
concentraciones de iones de hidrógeno y los ácidos débiles tienen
concentraciones bajas. El pH, entonces, es un valor numérico que expresa
la concentración de iones de hidrógeno.
Hay centenares de ácidos. Ácidos fuertes, como el ácido sulfúrico,
que puede disolver los clavos de acero, y ácidos débiles, como el ácido
bórico, que es bastante seguro de utilizar como lavado de ojos. Hay
también muchas soluciones alcalinas, llamadas "bases", que pueden ser
soluciones alcalinas suaves, como la Leche de Magnesia, que calman los
trastornos del estómago, y las soluciones alcalinas fuertes, como la
soda cáustica o hidróxido de sodio, que puede disolver el cabello
humano.
Los valores numéricos verdaderos para estas concentraciones de
iones de hidrógeno marcan fracciones muy pequeñas, por ejemplo
1/10.000.000 (proporción de uno en diez millones). Debido a que números
como este son incómodos para trabajar, se ideó o estableció una escala
única. Los valores leídos en esta escala se llaman las medidas del
"pH".
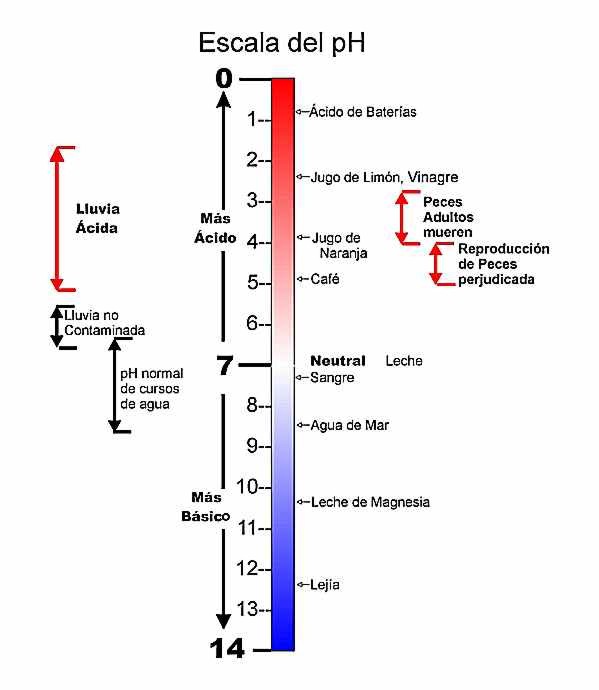 |
• La escala pH está dividida en 14 unidades, del 0 (la acidez
máxima) a 14 ( nivel básico máximo). El número 7 representa el nivel
medio de la escala, y corresponde al punto neutro. Los valores menores
que 7 indican que la muestra es ácida. Los valores
mayores que 7 indican que la muestra es básica.
• La escala pH tiene una secuencia logarítmica, lo que significa
que la diferencia entre una unidad de pH y la siguiente corresponde a
un cambio de potencia 10. En otras palabras, una muestra con un valor pH
de 5 es diez veces más ácida que una muestra de pH 6. Asimismo, una
muestra de pH 4 es cien veces más ácida que la de pH 6.
Cómo se mide el pH
Como cualquier medida, el pH posee una escala propia que indica con exactitud un valor.
La formula para medir el pH es logarítmica, no lineal, por lo que cada nivel del pH por debajo de 7 es 10 veces más ácido que el nivel que está encima de el, y del mismo modo, cada nivel de pH por encima de 7 es 10 veces más alcalino que aquel que está por debajo. Por ejemplo, un pH de 2 es diez veces más alcalino que un pH de 3; un Ph de 9 es diez veces más alcalino que un pH de 8. Esto significa que pequeños cambios en el pH tienen grandes consecuencias. Por ejemplo, la lluvia ácida, que generalmente tiene un pH entre 4.2 y 4.4 es más de diez veces más ácida que la lluvia normal, que usualmente tiene un pH de 5.6.
Ésta es una tabla que va del número cero al catorce, siendo de esta manera el siete el número del medio. Si el pH es de cero a seis, la solución es considerada ácida; por el contrario, si el pH es de ocho a catorce, la solución se considera alcalina.
Como cualquier medida, el pH posee una escala propia que indica con exactitud un valor.
La formula para medir el pH es logarítmica, no lineal, por lo que cada nivel del pH por debajo de 7 es 10 veces más ácido que el nivel que está encima de el, y del mismo modo, cada nivel de pH por encima de 7 es 10 veces más alcalino que aquel que está por debajo. Por ejemplo, un pH de 2 es diez veces más alcalino que un pH de 3; un Ph de 9 es diez veces más alcalino que un pH de 8. Esto significa que pequeños cambios en el pH tienen grandes consecuencias. Por ejemplo, la lluvia ácida, que generalmente tiene un pH entre 4.2 y 4.4 es más de diez veces más ácida que la lluvia normal, que usualmente tiene un pH de 5.6.
Ésta es una tabla que va del número cero al catorce, siendo de esta manera el siete el número del medio. Si el pH es de cero a seis, la solución es considerada ácida; por el contrario, si el pH es de ocho a catorce, la solución se considera alcalina.
Si la sustancia es más ácida, más cerca del cero estará; y entre más alcalina el resultado será más cerca del catorce. Si la solución posee un pH siete, es considerada neutra. Sin embargo el pH siete neutro se limita con seguridad, tan sólo a las soluciones acuosas, pues las que no son, si no están a una temperatura y presión normal, el valor de la neutralidad puede variar.
Hay distintas formas de medir el pH de una sustancia. La más sencilla es
sumergir un papel indicador o tornasol en la solución durante varios segundos y
éste cambiará de color según si es ácida (color rosa) o alcalina (color azul).
Este método no es tan preciso como otros, pues indica ambiguamente qué tan ácida
o qué tan alcalina es la sustancia, pese a la evolución que han experimentado
los papeles en cuanto a su exactitud.
Otra desventaja que presentan los papeles tornasol es que no pueden ser utilizados para ciertas sustancias, como por ejemplo, aquellas que son muy coloreadas o turbias.
Otra desventaja que presentan los papeles tornasol es que no pueden ser utilizados para ciertas sustancias, como por ejemplo, aquellas que son muy coloreadas o turbias.
La manera más exacta para la medición del pH, es utilizando un pHmetro y dos
electrodos, uno de referencia y otro de cristal. Un pHmetro es un voltímetro que
junto con los electrodos, al ser sumergidos en una sustancia, generan una
corriente eléctrica. Esta corriente eléctrica dependerá de la concentración de
iones de hidrógeno que presente la solución. El pHmetro mide la diferencia de
potencial entre el electrodo de referencia (plata) y el de cristal que es
sensible a los iones de hidrógeno. Para obtener con exactitud el pH de una
sustancia, se debe calibrar el pH con soluciones de valores de pH llamadas
buffer que resisten los cambios experimentados por el pH y tiene un valor de
pH específico.
El pH en la alimentación
Al ingerir alimentos alteramos el pH de nuestro cuerpo. El pH de nuestro estómago es de 1.4 debido al ácido que contiene y que es útil para descomponer los alimentos.
Algunas comidas y sus combinaciones pueden provocar que el estómago genere más ácido. Si esto sucede con mucha frecuencia, el ácido podría perforar el estómago causando una úlcera. Demasiado ácido en el estómago podría escapar hacia el esófago y llegar hasta tu boca. Esta desagradable sensación se conoce como acidez. Debes tener en cuenta los alimentos que injieres.
Neutralizando ácidos y álcalis
Las combinaciones de ácidos y álcalis (bases) se neutralizan automáticamente. Para atacar la acidez en el estómago, los médicos recomiendan tomar un anti-ácido. Los antiácidos, que químicamente son una base, neutralizan el ácido estomacal produciendo mejoría. También el bicarbonato de sodio tiene el mismo efecto.
El pH en el ambiente
El pH de la humedad del suelo afecta la disponibilidad de nutrientes para las plantas. Muchas plantas prefieren un suelo ligeramente ácido (pH entre 4.5 y 5.5), mientras que otras prefieren un suelo menos ácido (pH entre 6.5 y 7).
Los suelos altamente ácidos (con un pH menor de 4.5) alcanzan concentraciones de elementos químicos tóxicos para las plantas.
El pH del agua afecta la vida terrestre y acuática. El agua de los lagos, lagunas y ríos sanos generalmente tiene un pH entre 6 y 8. La mayoría de los peces tolera el agua con pH entre 6 y 9. Los peces más robustos y fuertes generalmente mueren en pH más bajos y más altos. Los sapos y otros anfibios son más sensibles al pH que muchos peces.
El pH puede servirnos para saber cuándo una sustancia es muy peligrosa para la vida.
El pH en tu boca
Después de cepillar tus dientes, el pH de la saliva en la boca, debe encontrarse con un valor alrededor de 7. Es decir un pH neutro, que no produce ningún daño a tus dientes.
Si el pH se encuentra debajo de 5.5, el esmalte comienza a perderse haciendo daño. Si comes algún carbohidrato, como pan o algo que contenga azúcar, este tendrá las condiciones para hacer más daño a los dientes.
Cuando un pedazo pequeño de alimento se descompone en la boca, genera gérmenes que la hacen más ácida, deteriorándolo más.
Para reducir los efectos dañinos a los dientes, las encías y mantener una boca sana; es muy importante el cepillado después de cada comida. Recuerda también utilizar el hilo dental y algún enjuague bucal.
La medida del pH se utiliza además en otros contextos: en los suelos, en las tierras, en las piscinas, en determinados análisis clínicos (sangre y orina), en el cabello y productos de cosmética y estética....
El pH en la alimentación
Al ingerir alimentos alteramos el pH de nuestro cuerpo. El pH de nuestro estómago es de 1.4 debido al ácido que contiene y que es útil para descomponer los alimentos.
Algunas comidas y sus combinaciones pueden provocar que el estómago genere más ácido. Si esto sucede con mucha frecuencia, el ácido podría perforar el estómago causando una úlcera. Demasiado ácido en el estómago podría escapar hacia el esófago y llegar hasta tu boca. Esta desagradable sensación se conoce como acidez. Debes tener en cuenta los alimentos que injieres.
Neutralizando ácidos y álcalis
Las combinaciones de ácidos y álcalis (bases) se neutralizan automáticamente. Para atacar la acidez en el estómago, los médicos recomiendan tomar un anti-ácido. Los antiácidos, que químicamente son una base, neutralizan el ácido estomacal produciendo mejoría. También el bicarbonato de sodio tiene el mismo efecto.
El pH en el ambiente
El pH de la humedad del suelo afecta la disponibilidad de nutrientes para las plantas. Muchas plantas prefieren un suelo ligeramente ácido (pH entre 4.5 y 5.5), mientras que otras prefieren un suelo menos ácido (pH entre 6.5 y 7).
Los suelos altamente ácidos (con un pH menor de 4.5) alcanzan concentraciones de elementos químicos tóxicos para las plantas.
El pH del agua afecta la vida terrestre y acuática. El agua de los lagos, lagunas y ríos sanos generalmente tiene un pH entre 6 y 8. La mayoría de los peces tolera el agua con pH entre 6 y 9. Los peces más robustos y fuertes generalmente mueren en pH más bajos y más altos. Los sapos y otros anfibios son más sensibles al pH que muchos peces.
El pH puede servirnos para saber cuándo una sustancia es muy peligrosa para la vida.
El pH en tu boca
Después de cepillar tus dientes, el pH de la saliva en la boca, debe encontrarse con un valor alrededor de 7. Es decir un pH neutro, que no produce ningún daño a tus dientes.
Si el pH se encuentra debajo de 5.5, el esmalte comienza a perderse haciendo daño. Si comes algún carbohidrato, como pan o algo que contenga azúcar, este tendrá las condiciones para hacer más daño a los dientes.
Cuando un pedazo pequeño de alimento se descompone en la boca, genera gérmenes que la hacen más ácida, deteriorándolo más.
Para reducir los efectos dañinos a los dientes, las encías y mantener una boca sana; es muy importante el cepillado después de cada comida. Recuerda también utilizar el hilo dental y algún enjuague bucal.
La medida del pH se utiliza además en otros contextos: en los suelos, en las tierras, en las piscinas, en determinados análisis clínicos (sangre y orina), en el cabello y productos de cosmética y estética....



No hay comentarios:
Publicar un comentario